Cliquez sur un pictogramme pour aller directement à la rubrique le concernant.
Ce médicament n'appartient à aucun groupe générique
 Comprimé (Composition pour Un comprimé)
Comprimé (Composition pour Un comprimé)
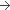 95,4 mg
95,4 mg
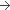 80 mg
80 mg
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 20/12/2023 | Réévaluation SMR et ASMR | Le service médical rendu par TAGRISSO (osimertinib) reste important uniquement en monothérapie dans le traitement adjuvant après résection tumorale complète et après chimiothérapie adjuvante si indiquée des patients adultes atteints dun cancer bronchique non à petites cellules (CBNPC) de stades IB IIIA avec mutations activatrices du récepteur du facteur de croissance épidermique (EGFR) par délétion de lexon 19 ou substitution de lexon 21 (L858R). |
| Important | Avis du 19/01/2022 | Extension d'indication | " Le service médical rendu par TAGRISSO (osimertinib) est : - Important uniquement en monothérapie dans le traitement adjuvant après résection tumorale complète et après chimiothérapie adjuvante si indiquée des patients adultes atteints dun cancer bronchique non à petites cellules (CBNPC) de stade IB IIIA avec mutations activatrices du récepteur du facteur de croissance épidermique (EGFR) par délétion de lexon 19 ou substitution de lexon 21 (L858R). " |
| Insuffisant | Avis du 19/01/2022 | Extension d'indication | Insuffisant pour justifier dune prise en charge par la solidarité nationale dans les autres situations. |
| Important | Avis du 20/03/2020 | Extension d'indication | Le service médical rendu par TAGRISSO (osimertinib) est important dans cette extension dindication de lAMM. |
| Important | Avis du 13/09/2017 | Réévaluation ASMR | Le service médical rendu par TAGRISSO est important dans le traitement des patients adultes atteints dun cancer bronchique non à petites cellules (CBNPC) localement avancé ou métastatique, avec mutation EGFR T790M acquise lors dun traitement par ITK anti EGFR. |
| Important | Avis du 21/09/2016 | Inscription (CT) | Le service médical rendu par TAGRISSO est important dans lindication de lAMM. |
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Avis du 20/12/2023 | Réévaluation SMR et ASMR | TAGRISSO (osimertinib), en traitement adjuvant, apporte une amélioration du service médical rendu modérée (ASMR III) par rapport à la stratégie de prise en charge actuelle du CBNPC de stades IB-IIIA avec mutations activatrices de lEGFR par délétion de lexon 19 ou substitution de lexon 21 (L858R) après résection tumorale complète et chimiothérapie adjuvante si indiquée. | |
| Avis du 19/01/2022 | Extension d'indication | " Compte tenu de : - la démonstration de la supériorité de losimertinib par rapport au placebo dans une étude de phase III, en double insu en termes de survie sans maladie avec une réduction significative : o chez les patients de stade II-IIIA (critère de jugement principal), HR=0,17 . IC99,06%[0,11 . 0,26] . p < 0,0001) et o chez les patients de stade IB-IIIA (population totale, critère de jugement secondaire hiérarchisé), HR= 0,20 . IC99,12% [0,14 . 0,30] . p < 0,0001), et malgré : - limmaturité des données de survie globale pour conclure à un avantage de TAGRISSO (osimertinib) par rapport au placebo sur ce critère de jugement - le surcroit de toxicité par rapport au placebo avec notamment plus dévénements indésirables de grades = 3 (20,2% versus 13,4%) ou ayant conduit à larrêt du traitement (11% versus 2,9%), - labsence de données de qualité de vie à valeur démonstrative, La Commission considère que TAGRISSO (osimertinib), en traitement adjuvant, apporte une amélioratio |
|
| Avis du 20/03/2020 | Extension d'indication | " Compte tenu de : - la démonstration de la supériorité de losimertinib par rapport aux ITK anti-EGFR erlotinib ou géfitinib en termes de : o survie sans progression évaluée par linvestigateur (médiane de survie de 10,2 mois dans le groupe osimertinib vs 13,8 mois dans le groupe comparateur . HR=0,46 . IC95% [0,37 . 0,57] . p < 0,0001) et, o de survie globale (médiane de survie de 38,6 mois dans le groupe osimertinib vs 31,8 mois dans le groupe comparateur . HR=0,799 . IC95,05% [0,64 .0,99], p=0,0462), - la tolérance acceptable de losimertinib par rapport aux ITK anti-EGFR erlotinib ou géfitinib, - labsence de conclusion formelle pouvant être tirée des résultats de qualité de vie, la Commission considère que TAGRISSO (osimertinib) apporte une amélioration du service médical rendu modérée (ASMR III) par rapport aux ITK anti-EGFR TARCEVA (erlotinib) et IRESSA (géfitinib), dans la prise en charge du cancer bronchique non à petites cellules localement avancé ou métastatique avec mutations a |
|
| Avis du 13/09/2017 | Réévaluation ASMR | Prenant en compte : - la supériorité de losimertinib versus chimiothérapie établie en termes de survie sans progression (gain absolu de 5,7 mois), - le profil de tolérance plus favorable de losimertinib par rapport à la chimiothérapie à base dun sel de platine, - mais labsence de démonstration à ce jour dun gain en survie globale par rapport à la chimiothérapie - et le caractère ouvert de létude qui ne permet en particulier pas dapprécier le gain en qualité de vie, la Commission considère que TAGRISSO apporte une amélioration du service médical rendu mineure (ASMR IV) par rapport à la chimiothérapie associant un sel de platine au pemetrexed chez des patients ayant acquis la mutation EGFR T790M lors dun traitement antérieur par ITK anti EGFR. |
|
| V (Inexistant) | Avis du 21/09/2016 | Inscription (CT) | Prenant en compte les seules données disponibles non comparatives ne permettant pas de quantifier lapport thérapeutique de TAGRISSO et dans lattente des résultats de létude comparative versus la chimiothérapie, la Commission considère que TAGRISSO napporte pas damélioration du service médical rendu (ASMR V) dans la stratégie thérapeutique qui comprend les comparateurs cliniquement pertinents (cf. paragraphe dédié). |