Cliquez sur un pictogramme pour aller directement à la rubrique le concernant.

Ce médicament n'appartient à aucun groupe générique
 Solution (Composition pour Une seringue préremplie)
Solution (Composition pour Une seringue préremplie)
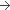 100 mg
100 mg
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Insuffisant | Avis du 30/03/2022 | Extension d'indication | Le service médical rendu par KINERET (anakinra) est insuffisant dans lindication de lAMM pour justifier une prise en charge par la solidarité nationale au regard des alternatives disponibles. |
| Important | Avis du 18/11/2020 | Extension d'indication | Le service médical rendu par KINERET (anakinra) est important dans le traitement des patients atteints de FMF ayant une résistance, une intolérance ou une contre-indication à la colchicine. |
| Important | Avis du 20/03/2019 | Extension d'indication | Le service médical rendu par KINERET est important dans lindication de lAMM. |
| Faible | Avis du 17/09/2014 | Inscription (CT) | Le service médical rendu par KINERET est faible dans lindication de la polyarthrite rhumatoïde en association avec le methotrexate. |
| Important | Avis du 17/09/2014 | Inscription (CT) | Le service médical rendu par KINERET est important dans le traitement des syndromes périodiques associés à la cryopyrine chez les adultes, les adolescents, les enfants et les bébés à partir de 8 mois et pesant au moins 10 kg. |
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 18/11/2020 | Extension d'indication | " Compte tenu : - de la supériorité par rapport au placebo dans létude clinique institutionnelle de Ben-Zvi et al. 2017 en termes de nombre moyen de crises mensuelles (1er critère de jugement principal) et des données observationnelles suggérant son intérêt clinique, mais considérant : - les limites méthodologiques de létude clinique et le faible niveau des données observationnelles, - labsence de données comparatives à ILARIS (canakinumab), seul comparateur cliniquement pertinent chez les patients résistants à la colchicine, - labsence de démonstration de la prévention de lamylose secondaire, complication majeure susceptible dengager le pronostic vital et, - le caractère quotidien des injections sous-cutanées de lanakinra comparativement aux injections mensuelles du canakinumab, KINERET (anakinra) napporte pas dAmélioration du Service Médical Rendu (ASMR V) dans la stratégie de prise en charge de la FMF chez les patients résistants, intolérants ou ayant une contre-indication à |
| V (Inexistant) | Avis du 20/03/2019 | Extension d'indication | " Considérant : - la supériorité de KINERET démontrée versus placebo après un mois de traitement en double aveugle dans létude Quartier et al. chez des patients en échec de la corticothérapie (faible effectif et courte durée), - labsence de données versus les autres biothérapies ayant une AMM en deuxième intention à savoir le canakinumab (autre anti-IL 1) et le tocilizumab (anti-IL6), ne permettant pas de le situer par rapport à ces derniers, - la place établie de KINERET dans la prise en charge de larthrite juvénile systémique (maladie rare) depuis de nombreuses années, la Commission considère que KINERET napporte pas damélioration du service médical rendu (ASMR V) dans la stratégie de prise en charge de lAJIs. Considérant : - la faiblesse méthodologique des données defficacité disponibles (étude ouverte nayant pas montré de différence versus traitement de fond [DMARD] chez un faible effectif de patients, études observationnelles sans groupe contrôle) ne permettant pas dappréci |
| V (Inexistant) | Avis du 17/09/2014 | Inscription (CT) | Ces spécialités sont des compléments de gamme qui napportent pas damélioration du service médical rendu (ASMR V, inexistante) par rapport aux autres présentations déjà inscrites, dans lindication : polyarthrite rhumatoïde en association avec le methotrexate. |
| Avis du 17/09/2014 | Inscription (CT) | Compte tenu de son efficacité montrée dans des formes sévères des cryopyrinopathies (syndrome CINCA/NOMID) malgré les limites méthodologiques des études disponibles, de sa capacité à passer la barrière hémato-encéphalique, de labsence dalternative thérapeutique chez les patients âgés de moins de 2 ans et malgré la nécessité dinjections quotidiennes, KINERET, comme ILARIS, apporte une amélioration du service médical rendu importante (ASMR II), dans le traitement des syndromes périodiques associés à la cryopyrine chez les adultes, les adolescents, les enfants et les bébés à partir de 8 mois et pesant au moins 10 kg. |