Cliquez sur un pictogramme pour aller directement à la rubrique le concernant.
Ce médicament n'appartient à aucun groupe générique
 Solution (Composition pour 1 mL de solution)
Solution (Composition pour 1 mL de solution)
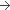 370 MBq à la date et à lheure de calibration
370 MBq à la date et à lheure de calibration
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 21/09/2022 | Réévaluation SMR et ASMR | Le service médical rendu par LUTATHERA (177Lutécium oxodotréotide) est important dans le traitement des tumeurs neuroendocrines pancréatiques inopérables ou métastatiques, pro-gressives, bien différenciées (G1 et G2) et exprimant des récepteurs de somatostatine chez les adultes. |
| Important | Avis du 29/06/2022 | Réévaluation ASMR | Le service médical rendu par LUTATHERA (177Lutécium oxodotréotide) reste important dans le traitement des tumeurs neuroendocrines intestinales inopérables ou métastatiques, progres-sives, bien différenciées (G1 et G2) et exprimant des récepteurs de la somatostatine chez les adultes. |
| Important | Avis du 11/07/2018 | Inscription (CT) | Le service médical rendu par LUTATHERA est important dans le traitement des tumeurs neuroendocrines intestinales « inopérables ou métastatiques, progressives, bien différenciées (G1 et G2) et exprimant des récepteurs de somatostatine chez les adultes ». |
| Insuffisant | Avis du 11/07/2018 | Inscription (CT) | Le service médical rendu par LUTATHERA est insuffisant pour justifier dune prise en charge par la solidarité nationale dans le traitement des TNE non intestinales « inopérables ou métastatiques, progressives, bien différenciées (G1 et G2) et exprimant des récepteurs de somatostatine chez les adultes ». |
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 21/09/2022 | Réévaluation SMR et ASMR | " Prenant en compte : ¿ la qualité peu robuste de la démonstration de lefficacité de LUTATHERA fondée sur les données dune étude de phase II non comparative, alors quune comparaison était possible vis-à-vis des alternatives déjà disponibles. Une (randomisation avec un groupe de contrôle interne de patients traités par sunitinib a été réalisée, sans possibilité de comparaison formelle à ce groupe . ¿ labsence de données issues dune comparaison externe avec une méthodologie adaptée . ¿ labsence de démonstration dun impact sur la survie globale . ¿ le besoin médical partiellement couvert . la Commission de la Transparence considère quen létat actuel du dossier, LUTATHERA (177Lutécium oxodotréotide) napporte pas damélioration du service médical rendu (ASMR V) dans la stratégie de prise en charge des patients adultes atteints dune tumeur neuroendocrine pancréatique inopérable ou métastatique, progressive, bien différenciée (G1 et G2) et exprimant des récepteurs de somatostatine. " |
| Avis du 29/06/2022 | Réévaluation ASMR | LUTATHERA (177Lutécium oxodotréotide) conserve une amélioration du service médical ren-du modérée (ASMR III) par rapport à loctréotide LP 60 mg administré seul, dans le traitement des tumeurs neuroendocrines intestinales inopérables ou métastatiques, progressives, bien différenciées (G1 et G2) et exprimant des récepteurs de la somatostatine chez les adultes. | |
| Avis du 11/07/2018 | Inscription (CT) | Prenant en compte : - la démonstration de la supériorité sur la survie sans progression de LUTATHERA, en association à loctréotide LP 30 mg, par rapport à loctréotide LP 60 mg seul, comparateur cliniquement pertinent (médiane non atteinte dans le groupe LUTATHERA, en association à loctréotide LP 30 mg et de 8,5 mois dans le groupe comparateur . HR = 0,18 . IC95% = [0,11 . 0,29] . p<0,0001), - une absence de différence en termes de survie globale entre les 2 groupes de traitement dans le cadre dune analyse intermédiaire conservatrice (médiane non atteinte dans le groupe LUTATHERA, en association à loctréotide LP 30 mg et de 27,4 mois dans le groupe comparateur avec HR =0,46 . IC95% = [0,25 . 0,83] et un p = 0,0083 > au seuil de significativité prédéfini au protocole), - les incertitudes sur la tolérance au long cours de la RIV avec LUTATHERA (notamment sur la myélotoxicité) et un profil de tolérance de lévérolimus qui semble plus défavorable, - du besoin médical à disposer dalternatives effi |