Cliquez sur un pictogramme pour aller directement à la rubrique le concernant.
Ce médicament n'appartient à aucun groupe générique
 Poudre (Composition pour Un flacon)
Poudre (Composition pour Un flacon)
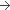 420 mg
420 mg
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 13/06/2018 | Inscription (CT) | Le service médical rendu par KANJINTI est identique à celui dHERCEPTIN dans chacune de ses indications, à savoir : Dans le traitement de patients adultes atteints d'un cancer du sein métastatique HER2 positif important : en association avec le paclitaxel, chez les patients non pré-traités par chimiothérapie pour leur maladie métastatique et chez lesquels le traitement par anthracyclines ne peut pas être envisagé . en association avec le docétaxel, chez les patients non pré-traités par chimiothérapie pour leur maladie métastatique. La Commission rappelle la nécessité dajouter le pertuzumab à lassociation KANJINTI/taxane en première ligne de traitement du cancer du sein métastatique HER2+. en association à un inhibiteur de l'aromatase, chez les patientes ménopausées ayant des récepteurs hormonaux positifs, non traitées précédemment par trastuzumab. Important dans « le traitement de patients adultes atteints d'un cancer du sein précoce HER2 positif : -après chirurgie, chim |
| Insuffisant | Avis du 13/06/2018 | Inscription (CT) | Le service médical rendu par KANJINTI est identique à celui dHERCEPTIN dans chacune de ses indications, à savoir insuffisant: Dans le traitement de patients adultes atteints d'un cancer du sein métastatique HER2 positif pour justifier une prise en charge par la solidarité nationale en monothérapie chez les patients pré-traités par au moins deux protocoles de chimiothérapie pour leur maladie métastatique, compte tenu du caractère désormais obsolète de cette indication dans la stratégie thérapeutique actuelle du cancer du sein métastatique HER2 positif. |
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 13/06/2018 | Inscription (CT) | En tant que médicament biosimilaire, KANJINTI napporte pas damélioration du service médical rendu par rapport à la biothérapie de référence, HERCEPTIN 150 mg, poudre pour solution à diluer pour perfusion (I.V.) (ASMR V). |