Cliquez sur un pictogramme pour aller directement à la rubrique le concernant.

Ce médicament n'appartient à aucun groupe générique
 Comprimé (Composition pour Un comprimé)
Comprimé (Composition pour Un comprimé)
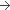 100 mg
100 mg
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 06/12/2023 | Réévaluation SMR et ASMR | Le service médical rendu par LYNPARZA (olaparib), en association au bévacizumab, reste important dans lindication de lAMM. |
| Important | Avis du 17/01/2024 | Réévaluation SMR et ASMR | Le service médical rendu par LYNPARZA (olaparib), en monothérapie, reste important dans lindication de lAMM. |
| Important | Avis du 05/04/2023 | Extension d'indication | Le service médical rendu (SMR) par LYNPARZA (olaparib) en association à labiratérone et à la prednisone ou à la prednisolone est important dans lextension dindication de lAMM. |
| Important | Avis du 18/01/2023 | Extension d'indication | Le service médical rendu par LYNPARZA (olaparib) est important dans cette extension dindication de lAMM. |
| Important | Avis du 05/05/2021 | Extension d'indication | Le service médical rendu par LYNPARZA (olaparib) est important dans cette nouvelle indication. |
| Important | Avis du 21/04/2021 | Extension d'indication | Le service médical rendu par LYNPARZA (olaparib), en association au bévacizumab, est important dans la nouvelle indication de lAMM. |
| Insuffisant | Avis du 16/12/2020 | Extension d'indication | Le service médical rendu par LYNPARZA (olaparib) est insuffisant pour justifier dune prise en charge par la solidarité nationale dans le reste de la population de lAMM : patients éligibles à la poursuite dun traitement de première ligne à base de platine, en labsence de données spécifiques disponibles. |
| Modéré | Avis du 16/12/2020 | Extension d'indication | Le service médical rendu par LYNPARZA (olaparib) est modéré dans la sous population de lAMM représentée par les patients atteints dun adénocarcinome du pancréas métastatique avec mutation germinale des gènes BRCA1/2 sans signes de progression après au minimum 16 semaines de chimiothérapie de première ligne à base de platine et qui ne sont pas éligibles à la poursuite à la poursuite de la chimiothérapie contenant des sels de platine. |
| Important | Avis du 11/12/2019 | Extension d'indication | Le service médical rendu (SMR) par LYNPARZA est important dans lindication de lAMM. |
| Important | Avis du 11/12/2019 | Extension d'indication | Le service médical rendu par LYNPARZA est important dans lindication de lAMM. |
| Important | Avis du 12/12/2018 | Inscription (CT) | Le service médical rendu par LYNPARZA est important dans lindication « en monothérapie pour le traitement d'entretien des patientes adultes atteintes dun cancer épithélial séreux de haut grade de l'ovaire, des trompes de Fallope ou péritonéal primitif, récidivant et sensible au platine avec une mutation du gène BRCA 1/2 (germinale et/ou somatique) et qui répondent (réponse complète ou réponse partielle) à une chimiothérapie à base de platine. ». |
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Avis du 06/12/2023 | Réévaluation SMR et ASMR | LYNPARZA (olaparib) en association au bévacizumab apporte une amélioration du service médical rendu modérée (ASMR III) par au bévacizumab en monothérapie dans le traitement dentretien des patientes adultes atteintes dun cancer épithélial avancé (stades FIGO III et IV) de haut grade de l'ovaire, des trompes de Fallope ou péritonéal primitif et qui sont en réponse partielle ou complète à une première ligne de traitement associant une chimiothérapie à base de platine au bévacizumab et dont le cancer est associé à un statut positif de la déficience en recombinaison homologue (HRD), défini par une mutation des gènes BRCA 1/2 et/ou une instabilité génomique. | |
| Avis du 17/01/2024 | Réévaluation SMR et ASMR | " Compte tenu : ¿ de la démonstration de la supériorité de lolaparib en monothérapie par rapport au placebo, dans une étude de phase 3 randomisée en double-aveugle, en termes de survie sans progression évaluée par linvestigateur : HR=0,30 [IC95% : 0,23-0,41], avec une médiane de survie sans progression non atteinte dans le groupe olaparib et de 13,8 mois dans le groupe placebo, ¿ de labsence de supériorité démontrée sur la survie globale, malgré les nouvelles données déposées, ¿ de labsence de conclusion formelle pouvant être tirée des résultats de qualité de vie, ¿ du profil de tolérance de lolaparib, avec notamment la survenue de syndromes myélodysplasiques/leucémies aiguës myéloïdes, la Commission considère que LYNPARZA (olaparib) en monothérapie apporte une amélioration du service médical rendu mineure (ASMR IV) dans la stratégie thérapeutique. " |
|
| Avis du 05/04/2023 | Extension d'indication | " Compte tenu : ¿ de la démonstration dune supériorité dans létude de phase III PROpel de lassociation olapa-rib + abiratérone par rapport au placebo + abiratérone, en termes de survie sans progression radiologique (avec soit une estimation ponctuelle dune différence absolue de médiane de SSPr de 8,2 mois avec un HR=0,66 . IC95% [0,54 . 0,81], p<0,0001) . et ce malgré : ¿ labsence de la démonstration de supériorité de lassociation olaparib + abiratérone par rapport au placebo + abiratérone sur la survie globale, ¿ un surcroit de toxicité ayant porté notamment sur les événements indésirables de grades = 3 avec 52,8% dans le groupe olaparib et 40,4% dans le groupe placebo, ¿ le risque de syndrome myélodysplasique (SMD) ou leucémie aiguë myéloïde (LAM), identifié comme risque important potentiel dans le plan de gestion des risques (PGR) et dans un con-texte de traitement à un stade avancé de la maladie, ¿ labsence de conclusion formelle pouvant être tirée sur la qualité de vie (critère |
|
| Avis du 18/01/2023 | Extension d'indication | " Compte tenu : ¿ de la démonstration dune supériorité dans létude de phase III OlympiA du traitement adjuvant olaparib (LYNPARZA) par rapport au placebo, en termes de : survie sans maladie invasive (avec 11,5 % des patients ayant présenté des événements de SSMI dans le groupe olaparib versus 19,5 % patients dans le groupe placebo, soit une différence de 9 points en faveur de lolaparib . HR=0,58 . IC 99,5 % [0,41 - 0,82], p=0,0000073) . survie globale (avec 8,1 % de patients décédés dans le groupe olaparib versus 11,9 % dans le groupe placebo, soit une différence absolue de 3,8 points en faveur de lolaparib . HR=0,68 . IC98,5% [0,47 - 0,97] . p=0,009) . et ce malgré : ¿ un surcroit de toxicité ayant porté notamment sur les événements indésirables de grades > 3 avec 24,5% dans le groupe olaparib versus 11,3% dans le groupe placebo . ¿ le risque de syndrome myélodysplasique (SMD) ou leucémie aiguë myéloïde (LAM), identifié comme risque important potentiels dans le plan de gestion des |
|
| Avis du 05/05/2021 | Extension d'indication | " Prenant en compte dune part : - la démonstration dune supériorité de lolaparib (LYNPARZA) par rapport à lenzalutamide ou à lacétate dabiratérone dans la cohorte A incluant trois mutations (BRCA 1, BRCA 2 et ATM) de létude de phase III ouverte PROFOUND avec un gain de +3,84 mois en médiane de survie sans progression radiologique (7,39 mois versus 3,55 mois) et de +4,40 mois en survie globale (19,09 mois versus 14,69 mois), et dautre part : - labsence de données comparatives versus la chimiothérapie par docétaxel pour les patients éligibles à ce traitement, - le surcroît de toxicité sous olaparib par rapport au groupe comparateur notamment en termes de fréquence des événements indésirables de grades = 3 rapportés chez 52% des patients du groupe olaparib et chez 40% dans le groupe comparateur), - labsence dimpact démontré sur la qualité de vie, la Commission considère que LYNPARZA (olaparib) apporte une amélioration du service médical rendu mineure (ASMR IV) par rapport à une hormo |
|
| Avis du 21/04/2021 | Extension d'indication | " Compte tenu : - des résultats, issus dune analyse en sous-groupe prévue a priori, mais non intégrée dans les méthodes de prise en compte de linflation du risque a global, suggérant la supériorité de lassociation olaparib + bévacizumab, par rapport au bévacizumab en monothérapie, en termes de survie sans progression (HR=0,33 [IC95% : 0,25-0,45]), avec des médianes respectives de 37,2 mois et 17,7 mois, dans une étude de phase III, randomisée, en double-aveugle . - et malgré : - un surcroît de toxicité avec la survenue dévénements indésirables de grades = 3 chez 34% des patientes, un arrêt définitif du traitement pour événement indésirable chez 18% des patientes et en particulier la survenue de leucémie aiguë myéloïde/syndrome myélodysplasique (identifiés comme risques importants potentiels dans le PGR). - labsence de démonstration dun gain en survie globale . - labsence de conclusion formelle pouvant être tirée des résultats de qualité de vie . la Commission de la Transparence consid |
|
| V (Inexistant) | Avis du 16/12/2020 | Extension d'indication | " Prenant en compte : - la démonstration dun gain en médiane de survie sans progression (critère de jugement principal) de +3,6 mois en faveur du groupe olaparib par rapport au placebo (7,4 mois versus 3,8 mois (HR=0,531 . IC95% [0,346 . 0,815]) dans une étude randomisée en double aveugle, - le besoin médical insuffisamment couvert dans ce cancer au pronostic très péjoratif, mais, - une absence de démonstration dun gain en survie globale, critère secondaire hiérarchisé (médiane de survie globale entre le groupe olaparib et le groupe placebo : 18,9 mois versus 18,1 mois, HR = 0,906 . IC95 % [0,563 . 1,457] . NS, - le choix du groupe comparateur dans létude : absence de traitement (placebo) à lissue dun nombre limité de cures de chimiothérapie en première ligne, très discutable car le traitement est en pratique poursuivi jusquà progression de la maladie ou intolérance, - le choix du critère de jugement principal (survie sans progression) dont la pertinence clinique est critiquable dans l |
| Avis du 11/12/2019 | Extension d'indication | " Prenant en compte : - la démonstration de la supériorité de lolaparib en termes de survie sans progression évaluée par linvestigateur par rapport au placebo (médiane non atteinte dans le groupe olaparib vs 13,8 mois dans le groupe placebo . HR = 0,30 . IC95% [0,23 . 0,41] . p < 0,0001), sans supériorité démontrée sur la survie globale lors de lanalyse intermédiaire prévue au protocole, - labsence de conclusion formelle pouvant être tirée des résultats de qualité de vie, - le profil de tolérance de lolaparib marqué principalement par des événements gastro-intestinaux et hématologiques et labsence de données de tolérance à long terme dans un contexte où ce médicament peut être administré de façon prolongée et que des cas dhémopathies malignes ont été rapportés, la Commission considère que LYNPARZA apporte une amélioration du service médical rendu mineure (ASMR IV) dans la stratégie thérapeutique de prise en charge des patientes adultes atteintes dun cancer épithélial avancé (stades FI |
|
| V (Inexistant) | Avis du 11/12/2019 | Extension d'indication | " Tenant compte : - dun gain démontré en termes de médiane de survie sans progression (critère de jugement principal) avec lolaparib versus une monochimiothérapie au choix de linvestigateur mais de pertinence clinique modeste de 2,9 mois (7,03 versus 4,17 mois . HR = 0,58 . IC95% [0,43 . 0,80] . p=0,0009), - de labsence de gain démontré sur la survie globale lors de lanalyse finale, - de labsence de donnée de qualité de vie à valeur démonstrative, la Commission considère que LYNPARZA (olaparib) napporte pas damélioration du service médical rendu (ASMR V) par rapport à une monochimiothérapie (capécitabine, vinorelbine ou éribuline). " |
| V (Inexistant) | Avis du 12/12/2018 | Inscription (CT) | LYNPARZA comprimé est un complément de gamme qui napporte pas damélioration du service médical rendu (ASMR V) par rapport à LYNPARZA gélule. |