Cliquez sur un pictogramme pour aller directement à la rubrique le concernant.
Ce médicament appartient au(x) groupe(s) générique(s) suivants :
 Comprimé (Composition pour Un comprimé)
Comprimé (Composition pour Un comprimé)
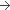 250 mg
250 mg
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Modéré | Avis du 25/06/2014 | Extension d'indication | Le service médical rendu par TYVERB est modéré dans « le traitement du cancer du sein, avec surexpression des récepteurs HER2 (ErbB2), en association au trastuzumab chez les patients ayant une maladie métastatique avec des récepteurs hormonaux négatifs, en progression après un (des) traitement(s) antérieur(s) par trastuzumab en association à une chimiothérapie. » |
| Important | Avis du 05/10/2011 | Inscription (CT) | Le service médical rendu par ces spécialités est important dans les indications de lAMM. |
| Important | Avis du 03/11/2010 | Inscription (CT) | Le service médical rendu par cette spécialité est important. |
| Important | Avis du 16/07/2008 | Inscription (CT) | Le service médical rendu par cette spécialité est important dans lindication de lAMM. |
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 25/06/2014 | Extension d'indication | TYVERB, en association au trastuzumab, napporte pas damélioration du service médical rendu (ASMR V, inexistante) par rapport à la prise en charge habituelle du cancer du sein avec surexpression des récepteurs HER2 (ErbB2) chez les patients ayant une maladie métastatique avec des récepteurs hormonaux négatifs. |
| V (Inexistant) | Avis du 05/10/2011 | Inscription (CT) | Ces spécialités sont un complément de gamme napportant pas damélioration du service médical rendu (ASMR V). |
| V (Inexistant) | Avis du 03/11/2010 | Inscription (CT) | Compte tenu de l'absence de comparaison avec l'association trastuzumab + inhibiteur de l'aromatase et en l'absence de données d'efficacité chez les patientes préalablement traitées par trastuzumab en adjuvant, Tyverb associé à un inhibiteur de l'aromatase n'apporte pas d'amélioration du service médical rendu (ASMR V) dans la stratégie thérapeutique du cancer du sein avec surexpression des récepteurs HER2 chez les patientes ménopausées ayant une maladie métastatique avec des récepteurs hormonaux positifs, pour lesquelles la chimiothérapie n'est actuellement pas envisagée et non préalablement traitées par trastuzumab. |
| Avis du 16/07/2008 | Inscription (CT) | Compte tenu d'une part, de l'amélioration observée par l'association TYVERB + XELODA par rapport à XELODA en monothérapie en termes de temps médian jusqu'à progression et d'un profil de tolérance acceptable, mais d'autre part, de l'absence de démonstration sur la survie globale, la Commission de la transparence considère que TYVERB, en association avec XELODA, apporte une amélioration du service médical rendu modérée (ASMR III) dans le traitement du cancer du sein avancé ou métastatique, avec surexpression des récepteurs HER2, chez les patientes en progression après un traitement antérieur ayant comporté une anthracycline, un taxane et le trastuzumab. |