GRANOCYTE 13 Millions UI/ml, poudre et solvant pour solution injectable/perfusion en seringue préremplie |
 |
|
Cliquez sur un pictogramme pour aller directement à la rubrique le concernant.

Ce médicament n'appartient à aucun groupe générique
 Poudre (Composition pour Un flacon)
Poudre (Composition pour Un flacon)
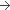 13,4 Millions UI (105 microgrammes)
13,4 Millions UI (105 microgrammes)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 18/09/2019 | Renouvellement d'inscription (CT) | Le service médical rendu par GRANOCYTE (lénograstim) reste important dans les indications de lAMM. |
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS . Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Avis du 21/06/2006 | Inscription (CT) | Pour les deux autres indications concernées : mobilisation des cellules souches périphériques chez les patients en vue d'une autogreffe et réduction de la durée de la neutropénie chez les patients recevant un traitement myélosuppresseur suivi de greffe de moelle et présentant un risque accru de neutropénies sévères et prolongées, la Commission considère que les deux facteurs de croissance, dont GRANOCYTE, ont toujours une place importante et occupent une place identique dans la stratégie thérapeutique | |
| Avis du 21/06/2006 | Inscription (CT) | Dans l'indication Mobilisation de cellules souches progénitrices chez les donneurs sains en vue d'une allogreffe, GRANOCYTE partage le niveau d'ASMR III accordé à NEUPOGEN. | |
| Avis du 05/05/2004 | Inscription (CT) | Ladministration des facteurs de croissance G-CSF, dont GRANOCYTE à des patients atteints de cancer, a constitué au début des années 1990, un progrès thérapeutique majeur. A ce jour, les facteurs de croissance G-CSF, dont GRANOCYTE, ont toujours une place importante dans la réduction des neutropénies sévères induites par les chimiothérapies, et occupent une place identique dans la stratégie thérapeutique. Il y a lieu de signaler que, contrairement à NEULASTA, GRANOCYTE peut être utilisé chez lenfant comme NEUPOGEN. Par ailleurs, GRANOCYTE comme NEUPOGEN doit être injecté tous les jours, contrairement à NEULASTA qui est administré en injection unique par cure. |